Herald-Lab
【물리학 - 열역학】 07. 기체분자운동론 <PART 1> 본문

이상기체분자의 거동
Behaviors of an Ideal Gas
기체분자운동론을 고전역학적으로 설명하는 데 있어 첫 번째 가정은 이상기체의 분자모형을 설정하는 것이다. 크게 5가지의 가정은 둔다.
- 기체의 분자 수는 무수히 많고 분자 사이의 평균거리가 분자의 자체 크기보다 훨씬 크다. ⇒ 기체분자의 부피는 무시하나 질량은 고려한다.
- 각 기체분자는 뉴턴의 운동법칙을 따르지만, 기체 간의 힘을 고려하지는 않아 마구잡이로 움직인다고 가정한다. ⇒ 기체 분자의 무질서 운동
- 탄성 충돌이 일어나는 동안 분자 사이에는 근거리 힘만 작용한다.
- 기체 분자는 벽과 탄성충돌(완성탄성충돌)을 한다. 이러한 충돌은 용기의 벽에 거시적인 물리량인 압력으로 반영된다.
- 기체 분자는 순수한 단일 물질로 용기 내의 모든 분자는 동일한 특성을 지닌다.

이상기체분자의 압력표현
한 변의 길이가 d인 정육면체의 부피가 V인 용기에 N개의 이상기체 분자가 있다고 하자. 이상기체분자 거동 모델링을 위한 첫 번째 목표는 이상 기체의 거시적인 변수인 압력 p를 미시적인 물리량으로 표현하는 것이다.
1단계: 특정 기체분자(i)의 용기에 대한 거동

질량이 m_0인 여러 기체분자들 중 x축의 속도성분을 가진 하나의 특정 분자(i)를 선택한다. 분자가 벽과 탄성충돌하면 벽의 질량이 분자의 질량에 비해 매우 크므로 벽에 수직인 분자의 속도 성분은 정반대[그림 2]가 된다.

벽의 충격량과 분자의 운동량 변화는 서로 같다. x축의 우측으로 일정한 속력을 가지고 움직이던 기체분자는 벽면에 충돌한 뒤, 같은 속력으로 왼쪽으로 튕기게 된다. 벽면은 기체에 대해 좌측으로 힘을 준 것과 같다[그림 3].

2단계: 두 번째 충돌
v_x, i의 속력을 가진 기체 분자가 벽과 충돌한 이후 같은 벽에 두 번째로 충돌하기 위해서는 x축으로 용기를 왕복해야만 한다. 용기의 한 변을 d로 가정했기 때문에 왕복한 거리는 2d가 되고 따라서 걸린 시간은 다음과 같이 계산된다.

기체 분자는 탄성충돌을 하기 때문에 속력이 일정하게 유지된다.
- Δt_sec: 첫 번째와 두 번째 충돌 사이의 시간 간격
3단계: 왕복 운동이 여러 번 반복될 때, 한 번 왕복하는 동안의 평균 운동량 변화는 충돌이 일어난 시간 간격 동안의 운동량 변화와 같다.
다음, 충돌 시 분자의 운동량을 변화시키는 힘인 충격력은 두 물체의 충돌순간인 Δt동안에 발생한다. x축으로 기체분자는 왕복운동 중 1회의 벽면 충돌을 갖는데, 이 때문에 '1회 충돌 시 기체분자의 운동량 변화'와 '충돌 이후 왕복 운동 중 1회 충돌 시 기체분자의 운동량 변화'는 서로 같은 의미이다.
- 기체가 정육면체의 용기 내부를 왕복하는 동안 벽이 작용한 평균력을 구할 수 있다.

분자가 용기 내부를 한 번 왕복하는 동안 충돌은 단 한 번 발생한다.
- 매 시간 간격에 대해 벽에 정확히 한 번의 충돌만 발생하므로 이 결과는 Δt의 배수가 되는 긴 시간 간격 동안 기체 분자에 작용하는 평균력이다.
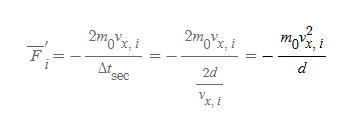
4단계: 단일 기체분자가 벽에 작용한 평균력
위의 내용은 벽이 기체 분자에 작용한 힘의 평균이므로 '기체분자가 벽에 작용한' 평균력은 부호만 반대인 아래와 같다.
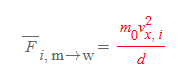
5단계: N개 기체분자가 벽에 작용한 평균력
하나의 특정한 분자 i를 넘어 N개의 기체가 벽에 작용한 전체 평균력은 각 분자가 벽에 작용한 힘을 모두 더한 것과 같다. 왜냐하면 모든 기체분자가 동일한 특성을 공유하기 때문이다.

또한 기체 분자의 수는 무수히 많기 때문에 시간에 따른 힘의 변화는 거의 무시될 정도가 된다. 그 이유는 어떠한 시간에서도 일정한 수의 분자가 용기에 부딫혀 일정한 힘의 평균을 만들기 때문이다. 따라서 기체분자는 벽에 대해 항상 일정한 힘을 작용하므로 1기체분자의 평균력이 곧 전체 기체분자의 힘이다.
6단계: 평균물리량과 기체분자의 속도 성분 확장
어떠한 집합에서의 평균 물리량이란, 집합 내의 모든 원소의 물리량을 합한 뒤 그 집합의 원소 수 N만큼을 나눈 값을 의미한다.

그리고 지금까지 설명한 모든 물리량은 x축으로만 이동하는 기체분자에 한정되었다. 기체분자는 3차원을 움직일 수 있으므로 개념을 확장하기 위해 [그림 1]처럼 모든 축을 이동할 수 있는 기체분자의 속도 성분을 분석해본다.

- 피타고라스의 정리에 따라 분자 속력의 제곱은 각 속도 성분의 제곱의 합과 같다.
분자속력 제곱의 평균 값 또한 위의 식과 비슷하다.
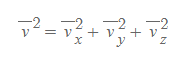
7단계: 기체분자의 무작위적 움직임
이상기체분자의 운동은 완전히 무작위적이므로 x, y, z축의 속도성분은 모두 동일한 것으로 취급된다.
- 기체분자가 완벽하게 한 차원의 속력 성분을 가지면 나머지 속력 성분은 무효가 된다. 따라서 3차원 상에서 3개의 축 중 하나를 고를 수 있을 때, 기체가 한 차원의 속력 성분을 선택할 확률은 전체 확률을 1로 두었을 때 1/3이 된다. 분자가 선택할 수 있는 축의 경우의 수가 3가지로 늘어났으므로 삼차원으로 움직이는 기체 분자에 대해 1/3을 곱하는 것은 매우 합리적이다.

8단계: 용기 벽에 작용하는 기체분자의 전체 힘과 압력
N개의 기체분자가 벽에 작용하는 평균력은 평균물리량의 개념에 따라 다음과 같이 식이 변형될 수 있다.
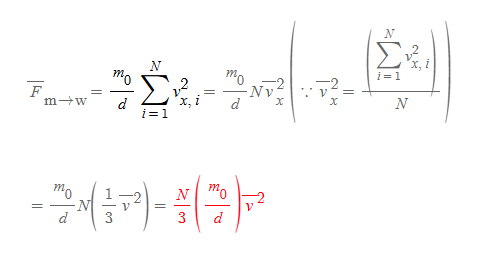
용기 벽에 작용하는 기체분자의 전체 힘

■
압력 p는 F/A의 기본 식을 따르고 면 A는 한 변의 길이가 d이므로 d^2로 계산된다.
용기 벽에 작용하는 기체분자의 전체 압력
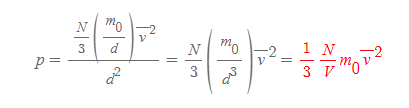
■
<물리량>
- V: 용기의 부피
'물리학 > 열역학' 카테고리의 다른 글
| 【물리학 - 열역학】 08. 기체분자운동론 <PART 2> (0) | 2025.11.09 |
|---|---|
| 【물리학 - 열역학】 06. 열전도 (0) | 2025.09.21 |
| 【물리학 - 열역학】 05. 열에너지 흐름(열류) (0) | 2025.09.20 |
| 【물리학 - 열역학】 04. 삼투압 (0) | 2025.08.01 |
| 【물리학 - 열역학】 03. 반데르발스 방정식 (0) | 2025.07.30 |