Herald-Lab
【물리학 - 열역학】 08. 기체분자운동론 <PART 2> 본문

기체분자의 속도와 속력
Velocity and Speed of Ideal Gases
앞선 챕터에서 우리는 x축상에서만 움직이는 기체 분자를 모델링의 대상으로 삼았다. 그리고 이를 3차원 상으로 전개하는 과정에서 분자속력제곱의 평균을 구했다.
이와 관련한 추가적인 설명과 함께 표기를 좀 더 쉽게 쓰도록 하자.
1단계: 속도 Vs. 속력
이미 고전역학에서 상세히 설명하였듯, 속도와 속력은 유의미한 개념 차이가 있다.
- 속도(velocity): 대상의 움직임 방향과 빠르기가 정해진 물리량
- 속력(speed): 대상의 빠르기
이를 수식으로 표현하면 다음과 같다.


[그림 1]과 같은 직교 좌표축에서 속도 v의 세 성분은 v_x, v_y, v_z로 나뉘며, 이 세 성분은 속력 v와는 피타고라스 정리에 의해 다음 관계를 만족한다.

2단계: 집합의 평균 물리량 - 속력 v_x^2의 평균
다음, 우리가 관심을 갖는 N개의 기체분자가 x축 상에서 용기와 상호작용을 하였을 때, 속력 v_x 제곱의 평균은 다음과 같다.

- 의미: N개 분자의 v_x^2값을 모두 더한 다음 N으로 나눈 값, 즉, 단일 기체가 갖는 x축에 대한 평균 속력 물리량
- 기체분자가 벽에 작용한 '평균'력을 계산하는 과정에서 속력의 제곱의 '평균'이 유의미해 졌다.
3단계: 집합의 평균 물리량 차원 확장
이상기체분자의 거동 특징 중 두 번째로 무질서 운동을 가정했다. 즉, 기체 분자들은 용기 내에서 선호하는 방향성이 없으므로 집합의 평균 물리량 또한 기체가 거동가능한 3가지 방향에 대해 (x-, y-, z-) 서로 같은 확률(값)으로 취급해야 한다.
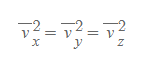
속력의 제곱의 평균 또한 피타고라스 정리처럼 쓸 수 있다.

기체분자의 평균운동에너지
Kinetic Energy of Ideal Gases
단일 기체분자의 질량이 m이라고 했을 때 용기 벽에 작용하는 기체분자 N개의 전체 압력 식에서 m(v^2)은 물체의 운동에너지인 (mv^2)/2과 연관시킬 수 있다.

단일 기체분자의 평균운동에너지
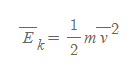
■
단일 기체분자의 평균운동에너지를 전체 압력 식에 반영하면 다음과 같다.

그리고 용기 벽에 작용하는 기체분자 N개의 전체 압력 p는 볼츠만 상수(Boltzmann constant)를 포함한 이상기체 상태방정식과도 연결되어 기체분자의 평균운동에너지를 온도 T만의 식으로 고쳐쓸 수 있다.
볼츠만 상수

■
<물리량>
- R: 기체상수
- N_A: 아보가드로 수, 약 6.022×10^23[개]
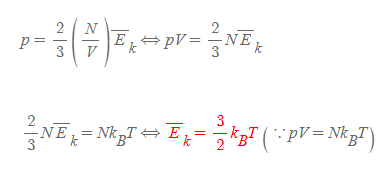

그림 2. ε로 표현된 기체분자의 평균운동에너지 [출처: University Physics for the Life Sciences (Knight et al, 1st ed., 2022, p.429)]
단일 기체분자의 평균운동에너지

■
단일 기체분자의 평균운동에너지는 기체 분자가 갖는 온도'만'의 값이다.

'물리학 > 열역학' 카테고리의 다른 글
| 【물리학 - 열역학】 07. 기체분자운동론 <PART 1> (0) | 2025.11.08 |
|---|---|
| 【물리학 - 열역학】 06. 열전도 (0) | 2025.09.21 |
| 【물리학 - 열역학】 05. 열에너지 흐름(열류) (0) | 2025.09.20 |
| 【물리학 - 열역학】 04. 삼투압 (0) | 2025.08.01 |
| 【물리학 - 열역학】 03. 반데르발스 방정식 (0) | 2025.07.30 |