728x90
반응형

열역학의 탐구 대상
Topics of Thermodynamics
열역학(thermodynamics): 거시적 계(system)에서 발생하는 에너지, 열, 그리고 일을 다루는 물리학의 한 분야
- 어원: 그리스어 therme(열) + dynamics(동력, 변화)
- 열역학 분야가 정립됨에 따라, 이후에는 엔트로피(entropy)와 과정의 자발성(spontaneous process)까지 포함하기도 한다.
- 열역학의 탐구 대상: 열, 일, 에너지, 온도, 엔트로피, 물질의 물리적 성질(physical properties of matter) 등
- 열역학의 탐구 대상은 열역학 법칙(laws of thermodynamics)의 지배를 받으며, 이를 통해 양적인 표현(quantitative description)이 가능하다.
- 열역학적 현상의 중요한 특징 중 하나는, 관찰하고자 하는 계와 이를 둘러싼 환경(surroundings) 사이의 에너지와 물질 교환은 항상 평형(equilibrium)을 이룬다는 점이다.
열역학은 다음과 같은 내용으로 응용 가능하다.
- 반응의 자발성: 어떠한 물리, 화학적 변화에 대한 방향성을 예측할 수 있다.
- 다양한 반응에 대한 에너지의 변화를 정량적으로 다룰 수 있게 한다.
- 공급되어진 열의 효율적 사용을 가능하도록 한다.
자발적 과정
자발적 과정(spontaneous process): 계에 대해 어떤 외부의 입력(external input)없이도 자체적으로 반응 등의 변화과정이 일어나는 현상
- 외부의 입력은 외력(external force) 등 외부로부터 오는 다양한 물리적 상호작용을 들 수 있다.
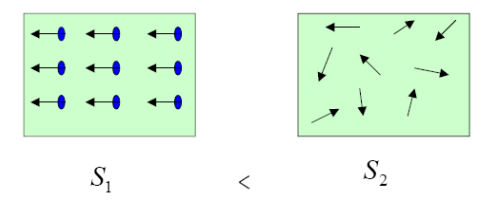
- 정량적인 자발적 과정은 열역학 제2법칙을 따르며, 이는 계와 주위의 엔트로피(S) 값이 커지는 방향으로 자발적 과정이 진행됨[그림 1]을 보여준다.
열역학사(史)
A Short History of Thermodynamics
열역학의 역사는 ‘열’이 ‘에너지’의 개념으로 해석되는 데서 출발한다.
- 독일의 물리학자 게리케(Otto von Guericke, 1602~1686)가 세계 최초의 진공펌프(vacuum pump)를 발명(1650)했다.
- 아일랜드 출신의 잉글랜드 물리학자 로버트 보일(Robert Boyle, 1627-1691)은 게리케의 진공펌프를 발전시키면서, 기체의 압력과 부피가 서로 반비례함을 공식화함(1662)
- 영국령 북아메리카 출신 물리학자 럼퍼드 백작(Benjamin Thompson, 1753~1814)이, 열을 물질의 일종으로 간주한 열소이론(caloric theory)을 실험적으로 논파함(1789)



- 1761년, 스코틀랜드의 물리학자 조셉 블랙(Joseph Black, 1728-1799)이 얼음의 상태변화를 연구하던 중, 물체의 상(phase)을 변화시키는 잠열(latent heat)의 개념을 추론함
- 1801년, 잉글랜드의 화학자 돌턴(John Dalton, 1766~1844)이 모든 기체는 온도가 증가함에 따라 그 부피가 일정하게 증가함을 발견
- 프랑스의 화학자 게이뤼삭(Joseph Louis Gay-Lussac, 1778~1850)이 모든 기체의 부피가 0이 되는 온도를 외삽법(extrapolation)을 활용해 예측했고, 절대온도 0K을 추론(1808)
- 1820년대에는 화학 실험을 통해 원자의 존재와 그 특성을 간접적으로 추론하였는데, 화학반응으로 인한 물질합성의 반응비를 확인할 수 있게 되었다.
- 1827년, 스코틀랜드의 식물학자 로버트 브라운(Robert Brown, 1773~1858)이 브라운 운동(Brownian motion)을 보고함 ⇒ 계의 확산현상에 대한 과학적 연구가 시작



- 독일의 물리학자 클라우지우스(Rudolf Julius Emanuel Clausius, 1822~1888)가 열역학 제2법칙을 정의함(1854) ⇒ "열은 고온의 물체에서 저온의 물체로 흐른다. 또한 스스로 저온부에서 고온부로 흐르지 않는다."
- 1873년, 네덜란드의 물리학자 반데르발스(판데르발스, Johannes van der Waals, 1837~1923)가 기체의 상태방정식(반데르발스 방정식, van der Waals’ equation)을 고안
- 미국의 수리물리학자 깁스(Josiah Willard Gibbs, 1839~1903)는 화학적 변화의 자발성을 결정하는 자유에너지(깁스에너지, free energy, Gibbs’s energy)를 유도(1878)했다. 뿐만 아니라 현대열역학의 수학적 해석에도 지대한 공을 남겼다.



728x90
반응형
'고급물리학 > 열역학' 카테고리의 다른 글
| [물리학-열역학] 06. 열역학 법칙: 이상기체 상태방정식 | Fundamental of Thermodynamics: The Ideal-gas Equation (0) | 2023.11.08 |
|---|---|
| [물리학-열역학] 05. 열역학 법칙: 기본개념 | Fundamental of Thermodynamics: Basic Concepts (0) | 2023.10.25 |
| [물리학-열역학] 04. 열응력 | Thermal Stress (0) | 2023.10.15 |
| [물리학-열역학] 03. 열팽창 | Thermal Expansion (0) | 2023.10.04 |
| [물리학-열역학] 02. 온도와 온도계 | Temperature and Thermometer (0) | 2023.09.30 |