
실제 기체와 반데르발스 방정식
Real Gases and Van der Waals's Equation
[열역학_06. 열역학 법칙: 이상기체 상태방정식]에서 배운 내용을 토대로 우리는 이상기체의 특징에 대해서 다음과 같이 정리할 수 있다.
[물리학-열역학] 06. 열역학 법칙: 이상기체 상태방정식 | Fundamental of Thermodynamics: The Ideal-gas Equation
이상기체 이상기체(ideal gases): 기체의 상태방정식(equations of state)에 완벽하게 기인하여 거동하는 ...
blog.naver.com
- 이상기체는 기체 분자 간의 인력이 작용하지 않고, 기체 분자 자체의 부피는 0인 기체이다.
- 이상기체는 이상기체 상태방정식을 만족하게 거동한다.
- 이상기체는 모든 압력에 걸쳐 보일의 법칙을 잘 만족한다.[그림 1]
3번의 내용은 pV=nRT의 식으로 부터 pV/nRT=Z라고 간주했을 때, 어떠한 압력에서도 값(상수) Z를 만족함을 의미한다.
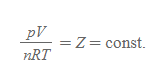
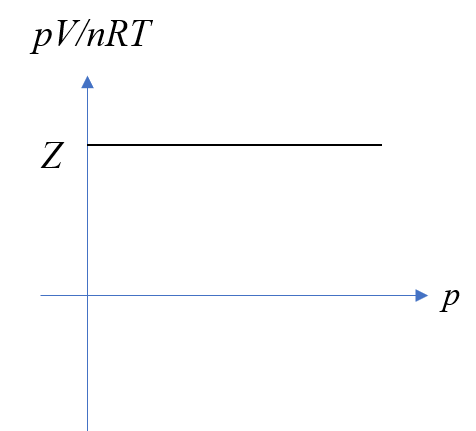
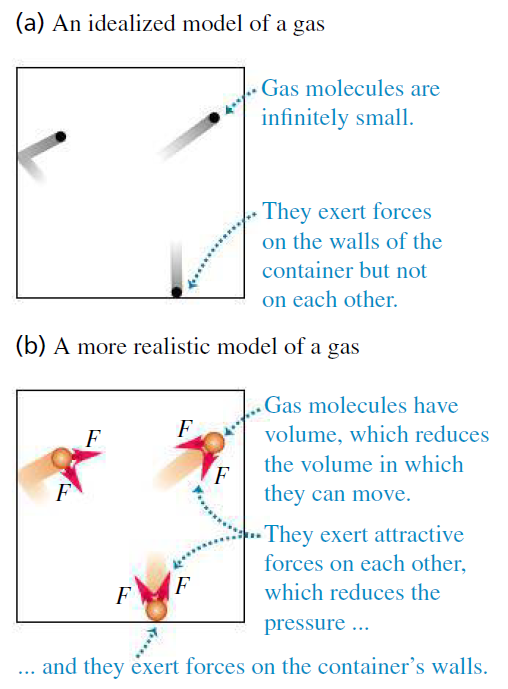
이상의 이상기체의 특징들에 대해 여러가지 반례들을 실제 기체로부터 발견[그림 2]할 수 있다.
- 실제 기체는 기체 분자 자체의 질량과 부피가 존재하므로, 인력이 작용한다.
- 실제 기체의 기체분자 자체의 부피 때문에 분자 간의 거리가 매우 가까워지면, 분자 간의 반발력도 급격히 발생한다.
- 기체 분자 간의 반발력 때문에 더 이상 기체의 부피가 감소하기 어려워지면 이때부터 기체의 부피는 상수가 된다.
- 기체의 부피가 감소하기 어려워지는 시점에서 압력이 증가하더라도 pV 값은 거의 선형적으로 증가한다.
위의 특징은 분자량과 부피가 상대적으로 큰 기체 분자(메테인 등)에 적용된다. 반면 수소 분자와 같이 기체의 분자량이 더 작다면, 기체 분자 자체의 부피로 인한 반발력 요소가 바로 나타난다.
- 기체 분자의 분자량이 클 경우, 어느 정도 인력이 작용한 뒤에 반발력이 급격히 증가한다.
- 반면 기체의 분자량이 작을 경우, 작은 질량으로 인해 인력 인자는 거의 영향력이 없다.
반데르발스 방정식

19세기, 네덜란드의 물리학자 반데르발스(J. D. van der Waals, 1837~1923)가 고안한 실제기체에 대한 근사상태방정식으로 방정식의 형태는 아래와 같다.
반데르발스 방정식 | Van der Waals Equation
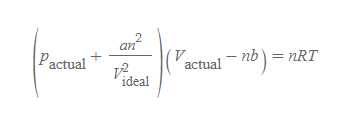
■
- 정의: 실제기체의 거동에 근사한 값을 유도하는 이상기체 상태방정식의 보정(식)
- 물리량
- p_actual: 기체 분자에 의한 실제 기체 압력 값
- V_actual: 기체 분자에 의한 실제 기체 부피 값
- a: 압력보정상수, 기체에 따라 다른 크기를 갖는 상수로, 분자들 사이의 인력 때문에 발생하는 실제 기체의 낮은 압력을 반영
- b: 부피보정상수, 기체에 따라 다른 크기를 갖는 상수로, 1몰의 분자들이 차지하는 기체 자체의 부피로
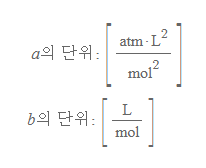
반데르발스 방정식의 유도
[1] n몰의 이상기체의 경우, 기체의 압력은 로 표현할 수 있다.

[2] 실제 기체는 (1)분자 자체의 부피와 함께 (2)분자 간의 상호작용이 존재하고, 분자 간의 상호작용은 대부분 분자간의 인력에 의한 것이다. ⇒ 실제 기체의 압력은 분자 간의 인력 요소로 이상기체에서 예상되는 압력보다 작게 측정된다.
- 기체 분자 간의 인력이 서로 작용함으로써 충돌 빈도가 낮아져 '이상기체'에서의 예측 값보다 작게 나온다.

[3] 기체의 감소되는 압력 p_d는 (1)이상기체가 차지할 수 있는 부피 V_actual의 제곱에 반비례하고, (2)기체의 몰수에는 제곱비례한다. → 비례상수(압력보정상수) a를 도입해 비례식을 항등식으로 만들 수 있다.
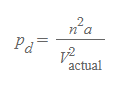
그러므로 p_actual은 다음과 같이 쓸 수 있다.
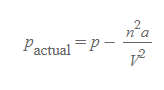
[4] 실제 기체 n몰개의 부피는 분자 자체의 부피요소로 이상 기체에서 예상되는 부피보다 크게 측정된다.
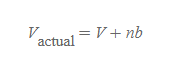
[5] pV=nRT 식은 이상기체가 가지는 p와 V에 대한 내용이었고, 이는 [과정 3]과 [과정 4]의 p_actual, V_actual 식을 변환하여 대입할 수도 있다.
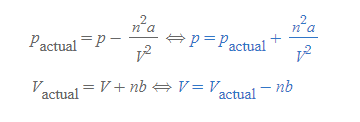
[6] 이상기체 상태방정식에 [과정 5]의 파란색 결과 값을 각각 대입하면 반데르발스 방정식이 최종 유도된다.
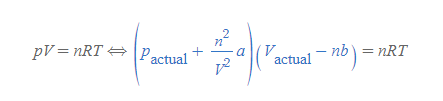
q.e.d.
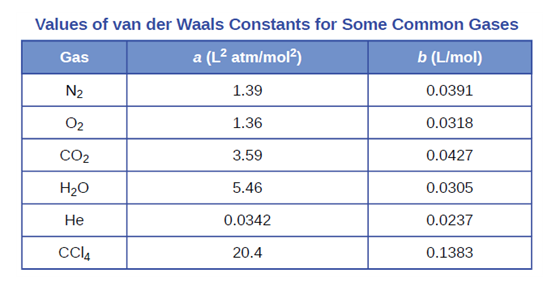
반데르발스 식의 보정상수[표 1]는 실험적으로 측정된다.
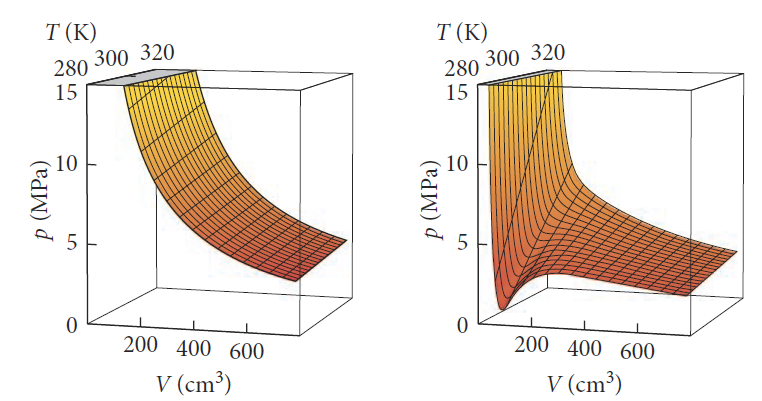
이상기체 상태방정식의 3차원 그래프의 모양 또한 반데르발스 방정식의 내용을 적용하면 [그림 3]과 같이 변한다.
'고급물리학 > 열역학' 카테고리의 다른 글
| [물리학-열역학] 09. 열역학 제1법칙: 기체가 한 일 | Work Done by Gases (0) | 2023.11.11 |
|---|---|
| [물리학-열역학] 08. 볼츠만 상수 | Boltzmann Constant (0) | 2023.11.10 |
| [물리학-열역학] 06. 열역학 법칙: 이상기체 상태방정식 | Fundamental of Thermodynamics: The Ideal-gas Equation (0) | 2023.11.08 |
| [물리학-열역학] 05. 열역학 법칙: 기본개념 | Fundamental of Thermodynamics: Basic Concepts (0) | 2023.10.25 |
| [물리학-열역학] 04. 열응력 | Thermal Stress (0) | 2023.10.15 |