728x90
반응형

열역학 제1법칙
The First Law of Thermodynamics
열역학 제1법칙: 에너지 보존법칙의 특수한 경우로, 열역학적 계에는 내부에너지의 변화만 일어나며 에너지는 열과 일에 의해서만 전달된다.
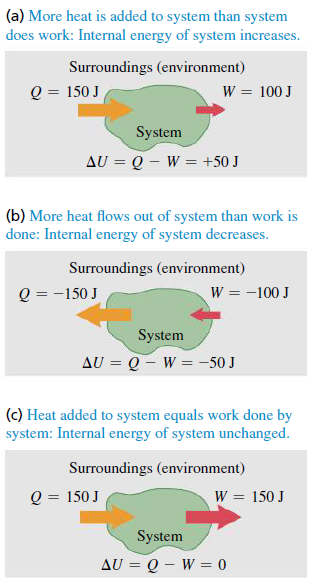
열역학 제1법칙 | The First Law of Thermodynamics
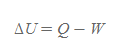
■
- 물리량
- ΔU: 열역학적 계가 가진 내부에너지
- Q: 열역학적 계로 출입하는 열
- W: 열역학적 계'가' 하는 일
열역학 제1법칙은 [그림 1]과 같이 열역학적 계(기체)가 주어가 되어 (1)이것의 내부에너지 변화량이 (2)시스템이 하는 일과 (3)시스템으로 출입하는 열 값에 의해 결정됨을 뜻한다.
- 기체의 내부에너지 변화는 기체 시스템으로 유출, 유입된 열 Q와 기체 시스템이 한 일 W에 의해 결정된다. ⇒ 기체 시스템에 대한 열에 기체 시스템이 한 일을 빼면 기체 시스템의 내부에너지를 구할 수 있다.
열역학 제1법칙의 부호
- 기체 시스템이 열을 받으면(유입) Q>0이다.
- 기체 시스템이 열을 방출하면(유출) Q<0이다.
- 기체가 든 피스톤이 팽창[그림 2]하면 ΔV>0이고, 기체가 한 일은 압력이 일정할 때 W=pΔV 식을 만족하기 때문에 W>0이다.
- 기체가 든 피스톤이 압축되면 ΔV<0이고, 기체가 한 일 식 때문에 W<0이다.
기체가 피스톤에 한 일 식을 열역학 제1법칙에 적용하면 부호를 이해하기 쉽다.
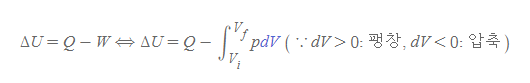
지금부터는 기체와 피스톤을 '피스톤-기체 시스템을 하나로 포함한 계'로 간주하여, [그림 1]과 같이 환경과 상호작용할 때의 기체 시스템의 열역학 제1법칙을 정리하자.
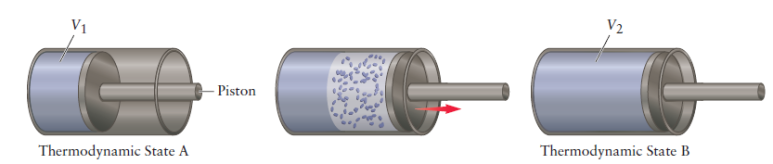
- [그림 3]과 같은 피스톤-기체 계는 자체의 내부에너지(internal energy)가 존재한다. 물체는 운동에너지, 퍼텐셜에너지 등 다양한 에너지를 포함하기 때문에 내부에너지 자체의 측정은 무의미한데, 대신 환경과의 상호작용으로 발생하는 내부에너지의 변화량은 측정 가능하다.
- [그림 3]과 같이 피스톤의 부피가 증가했을 때, 피스톤-기체 계는 '일을 했다', 즉, W>0로 표현할 수 있다.
- 피스톤-기체 계는 외부로부터 열 흐름(heat flow)을 받아 내부에너지의 변화량이 발생한다. 쉽게 말해 계가 열흐름을 받으면 Q>0이다.
제1법칙의 해석: 수입-지출모델
열역학 제1법칙의 식에서 계의 내부에너지 변화에 초점을 맞추면 다음과 같은 논리 구조를 갖는다.
- 계의 내부에너지 U는 마치 은행잔고와 같다. 따라서 ΔU>0는 수입으로, ΔU<0는 지출로 비유할 수 있다.
- 계의 내부에너지가 있을 때, 열을 방출(Q<0)하거나 실린더의 부피를 증가(ΔV>0)시켜 일을 할 수 있다.
- 따라서 피스톤-기체 계를 주어로 계가 열을 받거나(Q>0) 실린더의 부피가 압축(ΔV<0)되면 내부에너지의 '수입'이라 볼 수 있다.
- 열 출입이 없을 때, 피스톤-기체 계가 팽창하면 열역학 제1법칙의 식은 다음과 같다.
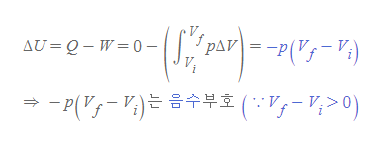
- 열 출입이 없을 때 피스톤이 팽창하면 ΔU는 음수가 되고 -pΔV만큼 값을 잃는다.
5. 열 출입이 없을 때, 피스톤-기체 계가 압축되면 열역학 제1법칙의 식은 다음과 같다.

- 열 출입이 없을 때 피스톤이 압축되면 ΔU는 양수가 되고 +pΔV만큼 값을 얻는다.
순환과정
순환과정(cyclic process): 계의 시작 상태와 끝이 동일한 열역학적 과정
- 순환조건의 두 가지 조건
- 내부에너지의 변화량은 0이다.
- Q=-W
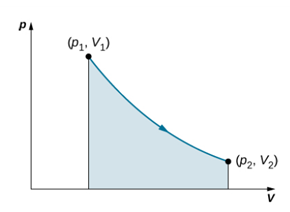
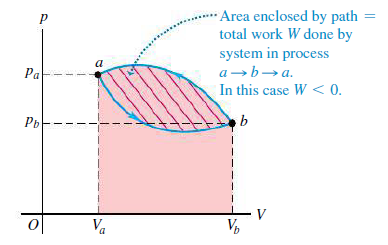
pV 도표에서 순환과정은 닫힌곡선으로 그려진다. ⇒ 한 순환과정에서 계에 한 알짜일은 도표 과정을 나타내는 경로로 둘러싸인 넓이[그림 4]와 같다.
728x90
반응형